 |
 |
 |

|
 |

 |
 |
 |

 |
 |
Рекомендации по выбору электродов |
 |
 |
 1. Введение в потенциометрию. 1. Введение в потенциометрию.
 2. Проблемы выбора электродов. Общие замечания. 2. Проблемы выбора электродов. Общие замечания.
 3. Ионометрия. Особенности выбора и эксплуатации электродов. 3. Ионометрия. Особенности выбора и эксплуатации электродов.
 4. pH-метрия. Особенности выбора электродов. 4. pH-метрия. Особенности выбора электродов.
 5. Измерение pH. Электродная пара или комбинированный электрод 5. Измерение pH. Электродная пара или комбинированный электрод
 (ЭС-1 + ЭСр-1 или ЭСК-1). (ЭС-1 + ЭСр-1 или ЭСК-1).
 6. Электроды сравнения. 6. Электроды сравнения.
 7. Рекомендуемая литература 7. Рекомендуемая литература

|
 |

2. Проблемы выбора электродов. Общие замечания.
 |

 Оптимальный подбор электродов для выполнения конкретной задачи достаточно сложная проблема. Необходимо учесть множество факторов, таких как: Оптимальный подбор электродов для выполнения конкретной задачи достаточно сложная проблема. Необходимо учесть множество факторов, таких как:

 1. Параметры анализируемой среды 1. Параметры анализируемой среды
 a. Диапазон концентраций анализируемого иона a. Диапазон концентраций анализируемого иона
 b. Температура и диапазон ее изменения, если она переменная b. Температура и диапазон ее изменения, если она переменная
 c. Наличие мешающих ионов c. Наличие мешающих ионов
 d. Наличие веществ агрессивных к материалу электрода d. Наличие веществ агрессивных к материалу электрода
 e. Ограничения на объем пробы e. Ограничения на объем пробы
 f. Физическое состояние анализируемого материала f. Физическое состояние анализируемого материала
 2. Методика анализа 2. Методика анализа
 a. Метод - прямая потенциометрия, потенциометрическое титрование или методы добавок a. Метод - прямая потенциометрия, потенциометрическое титрование или методы добавок
 b. Режим измерений - непрерывный или периодический b. Режим измерений - непрерывный или периодический
 3. Точность измерений 3. Точность измерений
 4. Требования и ограничения со стороны применяемых измерительных приборов и прочего оборудования 4. Требования и ограничения со стороны применяемых измерительных приборов и прочего оборудования
 a. Габаритные размеры электродов a. Габаритные размеры электродов
 b. Конфигурация электродов и форма чувствительной мембраны b. Конфигурация электродов и форма чувствительной мембраны
 c. Длина соединительного кабеля и тип разъема c. Длина соединительного кабеля и тип разъема

 Таким образом, задача выбора электродов сводится к поиску электродов, параметры которых удовлетворяют перечисленным требованиям и условиям. Задача осложнена тем, что некоторые из них взаимосвязаны. В том случае, если таких электродов нет, придется искать компромиссный вариант или другой метод измерения. Таким образом, задача выбора электродов сводится к поиску электродов, параметры которых удовлетворяют перечисленным требованиям и условиям. Задача осложнена тем, что некоторые из них взаимосвязаны. В том случае, если таких электродов нет, придется искать компромиссный вариант или другой метод измерения.
 Основной характеристикой измерительного электрода является диапазон определения. За диапазон определения принимают такую область электродной функции, в которой отклонения от линейности не превышают некоторую заданную величину, например pX=0,2. Причины возникновения отклонений от линейности в области высоких и низких концентраций определяемых ионов для разных электродов могут быть различными. Основной характеристикой измерительного электрода является диапазон определения. За диапазон определения принимают такую область электродной функции, в которой отклонения от линейности не превышают некоторую заданную величину, например pX=0,2. Причины возникновения отклонений от линейности в области высоких и низких концентраций определяемых ионов для разных электродов могут быть различными.
 В идеальном случае диапазон измерения электрода должен охватывать диапазон возможных концентраций анализируемых растворов. Если же требуется анализ растворов более концентрированных, чем это позволяет электрод, то пробу можно разбавить. Однако это легко реализуется только при периодических измерениях. Сложнее выполнить анализ растворов, содержащих исследуемое вещество на уровне ниже предела определения электрода, но и эта проблема в некоторых случаях может быть решена. Варианты решения будут изложены ниже. В идеальном случае диапазон измерения электрода должен охватывать диапазон возможных концентраций анализируемых растворов. Если же требуется анализ растворов более концентрированных, чем это позволяет электрод, то пробу можно разбавить. Однако это легко реализуется только при периодических измерениях. Сложнее выполнить анализ растворов, содержащих исследуемое вещество на уровне ниже предела определения электрода, но и эта проблема в некоторых случаях может быть решена. Варианты решения будут изложены ниже.
 Следующим по важности параметром идет температурный диапазон работы электрода. По этому параметру существует широкий выбор только для pH-электродов, для них доступна область измерений в пределах от 0 до 150°С. Для ионоселективных электродов модификаций с разными температурными диапазонами практически не бывает. В том случае, если не удается подобрать электроды с нужным температурным диапазоном, то проблема может быть решена нагревом или охлаждением анализируемого раствора. Это достаточно просто реализуется, в том числе и для непрерывных измерений. Следующим по важности параметром идет температурный диапазон работы электрода. По этому параметру существует широкий выбор только для pH-электродов, для них доступна область измерений в пределах от 0 до 150°С. Для ионоселективных электродов модификаций с разными температурными диапазонами практически не бывает. В том случае, если не удается подобрать электроды с нужным температурным диапазоном, то проблема может быть решена нагревом или охлаждением анализируемого раствора. Это достаточно просто реализуется, в том числе и для непрерывных измерений.
 Следует помнить, что электродная функция зависит от температуры (рис.1). Следует помнить, что электродная функция зависит от температуры (рис.1).

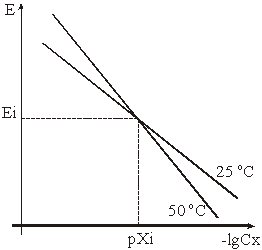 |
| Рис.1 |
|

 Сх - концентрация ионов Х; Сх - концентрация ионов Х;
 pXi = - lg (Cx) - в изопотенциальной точке; pXi = - lg (Cx) - в изопотенциальной точке;
 Ei - потенциал электрода в изопотенциальной точке. Ei - потенциал электрода в изопотенциальной точке.

 С увеличением температуры увеличивается наклон (крутизна St) электродной характеристики. С увеличением температуры увеличивается наклон (крутизна St) электродной характеристики.
 Концентрация анализируемых ионов, при которой потенциал электрода не зависит от температуры, называется изопотенциальной точкой. Значения концентрации раствора и потенциала электрода в этой точке называют координатами изопотенциальной точки (pXi и Ei). Концентрация анализируемых ионов, при которой потенциал электрода не зависит от температуры, называется изопотенциальной точкой. Значения концентрации раствора и потенциала электрода в этой точке называют координатами изопотенциальной точки (pXi и Ei).
 Для стеклянных электродов (pH и pNa) координаты изопотенциальной точки нормируется (указывается изготовителем), а для прочих измерительных электродов обычно нет. Современные измерительные приборы позволяют автоматически учитывать температурные изменения электродной характеристики (термокомпенсация), для этого в прибор должны быть введены координаты изопотенциальной точки и текущая температура. Последняя может вводиться либо вручную, либо посредством термодатчика, подключенного к прибору. Для стеклянных электродов (pH и pNa) координаты изопотенциальной точки нормируется (указывается изготовителем), а для прочих измерительных электродов обычно нет. Современные измерительные приборы позволяют автоматически учитывать температурные изменения электродной характеристики (термокомпенсация), для этого в прибор должны быть введены координаты изопотенциальной точки и текущая температура. Последняя может вводиться либо вручную, либо посредством термодатчика, подключенного к прибору.
 Если есть варианты, то рекомендуется выбирать электрод, имеющий изопотенциальную точку, лежащую вблизи средней концентрации анализируемых растворов. Это позволит снизить погрешность измерений, связанную с изменением температуры раствора. Если есть варианты, то рекомендуется выбирать электрод, имеющий изопотенциальную точку, лежащую вблизи средней концентрации анализируемых растворов. Это позволит снизить погрешность измерений, связанную с изменением температуры раствора.
 Очень внимательно следует отнестись к вопросу присутствия мешающих ионов и веществ, агрессивных к материалам электрода в анализируем растворе. Если они есть, то их удаление потребует специальной методики, а проведение непрерывных измерений будет, скорее всего, невозможным. Очень внимательно следует отнестись к вопросу присутствия мешающих ионов и веществ, агрессивных к материалам электрода в анализируем растворе. Если они есть, то их удаление потребует специальной методики, а проведение непрерывных измерений будет, скорее всего, невозможным.
 Потенциометрический анализ распространяется только на вещества, находящиеся в ионном состоянии, т.е. основной объект исследований это растворы (обычно водные), однако при этом растворы могут содержать взвеси твердых частиц, эмульсии, быть гелеобразными и т.д. Твердые материалы также могут быть исследованы этим методом при наличии специальной методики (растворение, экстрагирование и т.д.). Для исследования некоторых материалов может потребоваться электрод с определенной формой чувствительной мембраны, например конической для анализа гелей или вязких веществ. Потенциометрический анализ распространяется только на вещества, находящиеся в ионном состоянии, т.е. основной объект исследований это растворы (обычно водные), однако при этом растворы могут содержать взвеси твердых частиц, эмульсии, быть гелеобразными и т.д. Твердые материалы также могут быть исследованы этим методом при наличии специальной методики (растворение, экстрагирование и т.д.). Для исследования некоторых материалов может потребоваться электрод с определенной формой чувствительной мембраны, например конической для анализа гелей или вязких веществ.
 Потенциометрический метод анализа существует в нескольких вариантах: Потенциометрический метод анализа существует в нескольких вариантах:

 - Прямая потенциометрия. Метод основан на установлении зависимости потенциала измерительного электрода от концентрации раствора (построение калибровочного графика или настройка измерительного прибора) и последующим ее использовании для анализа растворов неизвестной концентрации. Метод достаточно прост и экспрессен. Наиболее широко применяется для измерения pH. Точность метода зависит, в первую очередь, от типа измерительного электрода. Так для pH-электродов достижима точность 0,01 pH и выше, а для ионоселективных электродов принято оценивать погрешность величиной 4% для однозарядных ионов и 8% для двухзарядных. Точность измерений так же заметно зависит от степени отклонения крутизны электродной функции от теоретического значения. Поэтому крутизна электродной функции является показателем качества электрода. Реальная крутизна электродной функции обычно равна или несколько ниже теоретического значения, превышение ее над теоретической величиной чаще всего говорит об ошибке эксперимента. Следует помнить, что со временем, по мере выработки ресурса электрода, крутизна снижается, и погрешности измерений возрастают. - Прямая потенциометрия. Метод основан на установлении зависимости потенциала измерительного электрода от концентрации раствора (построение калибровочного графика или настройка измерительного прибора) и последующим ее использовании для анализа растворов неизвестной концентрации. Метод достаточно прост и экспрессен. Наиболее широко применяется для измерения pH. Точность метода зависит, в первую очередь, от типа измерительного электрода. Так для pH-электродов достижима точность 0,01 pH и выше, а для ионоселективных электродов принято оценивать погрешность величиной 4% для однозарядных ионов и 8% для двухзарядных. Точность измерений так же заметно зависит от степени отклонения крутизны электродной функции от теоретического значения. Поэтому крутизна электродной функции является показателем качества электрода. Реальная крутизна электродной функции обычно равна или несколько ниже теоретического значения, превышение ее над теоретической величиной чаще всего говорит об ошибке эксперимента. Следует помнить, что со временем, по мере выработки ресурса электрода, крутизна снижается, и погрешности измерений возрастают.
 Достоинством и недостатком метода одновременно является то, что измеряемый потенциал зависит от активности. Это единственный метод прямого определения активности ионов в растворах. Но с другой стороны аналитиков чаще интересует концентрация, а пересчет активности ионов в концентрацию с применением эмпирических коэффициентов активности вызывает некоторую дополнительную погрешность. Существует вариант метода, в котором в калибровочные и анализируемые растворы вводится индифферентный электролит. Это позволяет проводить калибровку и последующий анализ в единицах концентрации. Достоинством и недостатком метода одновременно является то, что измеряемый потенциал зависит от активности. Это единственный метод прямого определения активности ионов в растворах. Но с другой стороны аналитиков чаще интересует концентрация, а пересчет активности ионов в концентрацию с применением эмпирических коэффициентов активности вызывает некоторую дополнительную погрешность. Существует вариант метода, в котором в калибровочные и анализируемые растворы вводится индифферентный электролит. Это позволяет проводить калибровку и последующий анализ в единицах концентрации.

 - Потенциометрическое титрование. Метод существует во множестве вариантов. Он основан на проведении специфической химической реакции под контролем ионоселективного или редокс-электрода. Могут применяться следующие реакции: нейтрализации, осаждения, комплексообразования или окисления-восстановления. Калибровка электрода обычно не требуется, он служит только для установления точки эквивалентности. Расчет концентрации анализируемого вещества производится на основании объемов и концентраций, участвующих в реакции растворов. - Потенциометрическое титрование. Метод существует во множестве вариантов. Он основан на проведении специфической химической реакции под контролем ионоселективного или редокс-электрода. Могут применяться следующие реакции: нейтрализации, осаждения, комплексообразования или окисления-восстановления. Калибровка электрода обычно не требуется, он служит только для установления точки эквивалентности. Расчет концентрации анализируемого вещества производится на основании объемов и концентраций, участвующих в реакции растворов.
 Метод более сложный и трудоемкий по сравнению с предыдущим, но имеет ряд преимуществ. Результаты, полученные этим методом, обычно более точны и воспроизводимы (<1%). Титрование позволяет определять вещества, на которые не существует ионоселективных электродов (косвенное определение). От применяемого электрода не требуется высокой линейности и стабильности характеристики. Правильный подбор реактивов позволяет проводить анализ в присутствии мешающих ионов. Метод более сложный и трудоемкий по сравнению с предыдущим, но имеет ряд преимуществ. Результаты, полученные этим методом, обычно более точны и воспроизводимы (<1%). Титрование позволяет определять вещества, на которые не существует ионоселективных электродов (косвенное определение). От применяемого электрода не требуется высокой линейности и стабильности характеристики. Правильный подбор реактивов позволяет проводить анализ в присутствии мешающих ионов.
 К недостаткам метода следует отнести невозможность его применения для непрерывного контроля, а так же то, что в ряде случаев им нельзя определять малые концентрации. К недостаткам метода следует отнести невозможность его применения для непрерывного контроля, а так же то, что в ряде случаев им нельзя определять малые концентрации.

 - Методы добавок. Родственный титрованию метод. Существует во множестве вариантов, некоторые из которых обладают преимуществами, существенно расширяющими область применения потенциометрии. Это, например, возможность анализа малых концентраций, лежащих на пределе линейности электродной характеристики, а иногда и ниже ("метод добавок с последующим разбавлением"). В присутствии избытка комплексообразующих агентов метод стандартных добавок является единственным методом, пригодным для определения общей концентрации ионов, входящих в состав комплексов. - Методы добавок. Родственный титрованию метод. Существует во множестве вариантов, некоторые из которых обладают преимуществами, существенно расширяющими область применения потенциометрии. Это, например, возможность анализа малых концентраций, лежащих на пределе линейности электродной характеристики, а иногда и ниже ("метод добавок с последующим разбавлением"). В присутствии избытка комплексообразующих агентов метод стандартных добавок является единственным методом, пригодным для определения общей концентрации ионов, входящих в состав комплексов.

|
 |
|
 |
 |
 |
|
